Cẩm nang bệnh cây - P14: Các phụ lục

P1 | P2 | P3 | P4 | P5 | P6 | P7 | P8 | P9 | P10 | P11 | P12 | P13 | P14
Phụ lục 1: Cách làm một que cấy dẹp
Que cấy dẹp là một trong những dụng cụ quan trọng nhất trong phòng thí nghiệm. Một que NiChrome (Nickel và Chromium Alloy, 80:20) đường kính 1 mm, thường dùng để tạo nóng trong máy sấy tóc, là vật liệu thích hợp nhất (Hình A1.1).
1. Cắt một đoạn dài 60mm.
2. Đập dẹp một đầu que tới khoảng ba lần bề ngang của que ban đầu. .
3. Dùng kìm hoặc kéo nặng cắt gọn phần que dẹp thành đầu nhọn.
4. Mài gọn phần đập dẹp.
5. Gắn que vào cán.
6. Hoàn tất que cấy dẹp.


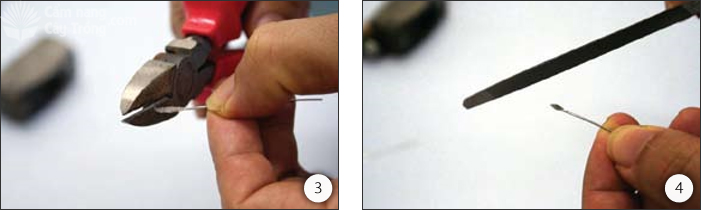

Hình A1.1 Hướng dẫn từng bước làm que cấy dẹp
Phụ lục 2: Sức khỏe và an toàn
Trên đồng ruộng
- Tuân thủ nghiêm ngặt tất cả các quy định về an toàn khi sử dụng thuốc trừ dịch hại, đặc biệt là thuốc trừ sâu. Chỉ dùng các hóa chất đã được đăng ký.
- Rửa tay cẩn thận trước khi ăn, nhất là sau các công việc có dính đất.
- Uống đủ nước vào những ngày nóng bức trên đồng ruộng.
- Cẩn thận với dao rựa để tránh cắt phạm vào chính mình hay người khác.
Trong phòng thí nghiệm
- Kiểm tra các chỉ dẫn an toàn của tất cả các hóa chất trước khi dùng. Có thể tìm thấy các thông tin đó trên bao bì sản phẩm hoặc từ mạng internet. Các công ty hóa chất lớn cung cấp các nối kết với Dữ liệu An toàn Vật liệu tương ứng với sản phẩm của họ.
- Dùng găng tay khi cần.
- Cồn êtyl rất dễ bắt lửa. Đừng lau bàn bằng cồn ở vị trí gần ngọn lửa.
- Giữ một chăn chống lửa trong phòng thí nghiệm để dập tắt cháy quần áo.
- Mang giày trong phòng thí nghiệm để bảo vệ tránh vật nhọn rơi lên chân. Giày kín cũng bảo vệ chân tránh thủy tinh vỡ và hóa chất.
- Không mở nồi hấp trước khi áp suất trong nồi trở lại bình thường (khi đồng hồ chỉ số 0). Luôn dùng găng tay dầy khi lấy bất cứ vật liệu gì từ nồi hấp hoặc tủ sấy.
- Cẩn thận khi mở tủ sấy. Nhiệt độ cao và hơi nước nóng có thể gây bỏng trầm trọng.
Phụ lục 3: Môi trường, khử trùng và bảo quản mẫu vi sinh vật
Phần môi trường bao gồm các công thức cho một số môi trường thông thường.. Có nhiều loại môi trường đã được tạo ra cho một số loài nấm hoặc quy trình thí nghiệm cụ thể. Những loại môi trường này được mô tả trong các tài liệu khoa học, nhất là trong các bài báo đăng các tạp chí khoa học.
Điều quan trọng là hiểu các nguyên tắc cơ bản trong việc khử trùng môi trường, dụng cụ thủy tinh và thiết bị khác bằng nhiệt. Thời gian xử lý cần được điều chỉnh cho phù hợp với số lượng và tính chất của vật liệu được khử trùng. Thời gian xử lý cũng khác nhau đáng kể giữa phương pháp khử trùng nóng ẩm (dùng nồi hấp) và nóng khô (dùng tủ sấy).
Có nhiều kỹ thuật bảo quản để lưu giữ mẫu nuôi cấy nấm. Một số phương pháp thông thường được trình bày trong phần này và nhiều phương pháp khác đã được nêu trong các tài liệu khác.
Có nhiều loại môi trường đã được tạo ra để nuôi cấy nấm. Trong số đó, có nhiều môi trường thích hợp cho việc nuôi cấy hầu hết các loại nấm như môi trường thạch nước cất (WA), môi trường thạch đường khoai tây (PDA). Các môi trường khác, như môi trường chọn lọc Phytophthora (PSM) và agar pentachloronitrobenzene peptone (PPA) là những môi trường chọn lọc dùng để phân lập một số nấm nhất định từ cây hoặc đất.
Môi trường tổng hợp, được làm hoàn toàn từ các hợp chất hóa học, có tính đồng nhất do cấu tạo hóa học của chúng là chuẩn. Các môi trường tự nhiên, như PDA
hoặc thạch cà rốt khoai tây (PCA), rẻ tiền và tạo điều kiện cho nấm phát triển tốt. Tuy nhiên, các môi trường tự nhiên (làm từ vật liệu tự nhiên, thường là các chất chiết thực vật) thay đổi tùy theo chất chiết từ cây. Nếu dùng môi trường tự nhiên để phân biệt đặc điểm hình thái hoặc tỷ lệ phát triển thì nên dùng cùng một mẻ môi trường cho tất cả các mẫu cấy. Một số môi trường tự nhiên như PDA có hàm lượng hyđrat-cacbon cao, làm cho sợi nấm khí sinh mọc nhanh. Nếu tiếp tục lặp lại việc cấy truyền trên những loại môi trường như vậy có thể làm cho nấm nhanh bị thoái hóa và mất độc tính. Vì vậy, nên dùng môi trường dinh dưỡng thấp để duy trì việc nuôi cấy.
 Trong khi khử trùng môi trường, nhớ nới lỏng nắp chai và vặn chặt sau khi đã khử trùng xong. Việc này tránh chai bị nổ trong điều kiện áp suất cao và tránh phải tốn nhiều công lau chùi.
Trong khi khử trùng môi trường, nhớ nới lỏng nắp chai và vặn chặt sau khi đã khử trùng xong. Việc này tránh chai bị nổ trong điều kiện áp suất cao và tránh phải tốn nhiều công lau chùi.
Nên dùng đĩa Petri thủy tinh trong những phòng thí nghiệm chẩn đoán nhỏ tại các vùng nhiệt đới. Kinh nghiệm cho thấy môi trường trong đĩa Petri thủy tinh sẽ ít bị nhiễm tạp bởi các bào tử từ không khí hơn so với môi trường trong đĩa nhựa.
A3.1. Một số nhận xét về thành phần môi trường
Nước
Nước máy phù hợp cho hầu hết các loại môi trường, bởi vì nước máy có chứa các chất vi lượng thường không có trong nước cất. Tuy nhiên, ở một số vùng nước máy có thể chứa độc tố đối với nấm. Một trong những chất đó là đồng có khả năng ức chế đối với nhiều loài nấm. Trong những trường hợp này tốt hơn hết là nên dùng nước cất.
Agar
Agar là chất chiết xuất từ tảo, và chất lượng thay đổi tùy thuộc vào nguồn gốc. Agar có thể ở dạng bột, dạng thỏi hoặc dạng lớp. Nhiều agar bột dễ tan trong khi hấp; các công thức nấu môi trường dưới đây đều sử dụng loại agar này.
Dùng loại agar chất lượng cao để môi trường, ví dụ môi trường thạch nước cất (WA), được trong. Môi trường WA dùng cho việc phân lập, cấy đơn bào tử, cấy đỉnh sinh trưởng sợi nấm và giám định cần phải trong suốt để có thể quan sát được sợi nấm và bào tử dưới kính lúp soi nổi.
 Chỉ dùng agar chất lượng thấp cho các môi trường không yêu cầu sự trong suốt, như PDA và PCA. Tuy nhiên nếu có thể tốt nhất không nên dùng agar chất lượng thấp.
Chỉ dùng agar chất lượng thấp cho các môi trường không yêu cầu sự trong suốt, như PDA và PCA. Tuy nhiên nếu có thể tốt nhất không nên dùng agar chất lượng thấp.
Thạch nước cất là môi trường phân lập đa năng hữu hiệu nhất. Không dùng PDA để phân lập nấm từ các bộ phận cây. Chỉ dùng PDA để nuôi cấy cho việc xác định đặc điểm hình thái tản nấm và sự hình thành sắc tố. Dùng các môi trường khác để kích thích việc sinh sản và hình thành bào tử, như mẩu lá hoặc thân, hoặc quả đậu tiệt trùng trong môi trường thạch nước cất. Các môi trường chọn lọc rất hữu dụng cho việc phân lập nấm từ rễ hoặc mô bệnh nặng bị tạp nấm hoại sinh và vi khuẩn.
Chất kháng sinh
Chất kháng sinh có thể được cho vào môi trường phân lập nấm để ngăn ngừa sự phát triển của vi khuẩn hoặc nấm không cần thiết (Bảng A3.1). Hầu hết các chất kháng sinh (ngoại trừ chloramphenicol; xem bên dưới) đều không bền nếu đun nóng do đó chỉ cho chất kháng sinh vào môi trường sau khi hấp khử trùng. Những chất kháng sinh này được hòa tan trong một lượng nhỏ nước cất sạch, tùy theo công thức. Đối với hầu hết các mục đích, chất kháng sinh có thể được thêm trực tiếp vào môi trường, nhưng đối với các thí nghiệm quan trọng, dung dịch kháng sinh cần được lọc tiệt trùng trước khi dùng.
Bảng A3.1. Các chất kháng sinh thông dụng
|
Chất kháng sinh |
Tác dụng kháng |
Tính hòa tan |
|
Penicillins |
Vi khuẩn Gram dương |
Tan trong nước |
|
Streptomycin |
Vi khuẩn Gram âm |
Tan trong nước |
|
Neomycin |
Vi khuẩn Gram dương |
Tan trong nước |
|
Chloramphenicol |
Vi khuẩn Gram dương và âm |
Tan trong Ethanol |
Chloramphenicol có thể thêm vào môi trường trước khi khử trùng. Chloramphenicol bị nghi gây ung thư, do đó cũng như tất cả các chất kháng sinh khác cần chú ý khi sử dụng.
Thuốc trừ nấm thường được dùng trong môi trường chọn lọc. Ví dụ loại nấm Fusarium có tính chịu tương đối với pentachloronitrobenzene (PCNB; Terrachlor® hoặc Quintozene) và dichloronitroaniline (DCNA; Allisan®) và những thuốc trừ nấm này được thêm vào môi trường chọn lọc cho Fusarium.
Rose Bengal được thêm vào một số môi trường dùng để phân lập nấm từ đất. Chất này ngăn cản việc phát triển của tất cả các loại nấm, và được thêm vào môi trường để ức chế các loài nấm mọc nhanh tràn lên các tản nấm của các loài nấm mọc chậm. Tính độc của Rose Bengal được tăng cường khi tiếp xúc với ánh sáng. Các đĩa môi trường Rose Bengal cần được cất giữ và ủ trong điều kiện bóng tối.
 Khi thêm vào môi trường, cần hòa tan hoàn toàn lượng chất kháng sinh này trong 10 mL nước tiệt trùng nhằm đảm bảo chất kháng sinh được phân bố đều trong môi trường. Khi cho vào môi trường (ở 55°C) chất kháng sinh cần được trộn vào môi trường bằng cách lắc cẩn thận để tránh tạo ra quá nhiều bọt.
Khi thêm vào môi trường, cần hòa tan hoàn toàn lượng chất kháng sinh này trong 10 mL nước tiệt trùng nhằm đảm bảo chất kháng sinh được phân bố đều trong môi trường. Khi cho vào môi trường (ở 55°C) chất kháng sinh cần được trộn vào môi trường bằng cách lắc cẩn thận để tránh tạo ra quá nhiều bọt.
Thường thì có nhiều loại môi trường khác nhau được dùng trong phòng thí nghiệm ở cùng một thời điểm. Do đó, tốt nhất là nên dùng bút mực màu không phai có màu sắc khác nhau đánh dấu ở thành đĩa Petri để dễ dàng phân biệt các loại môi trường khác nhau. Nên có một cách đánh dấu cố định cho mỗi loại môi trường khác nhau và dán trên tường phòng thí nghiệm để tránh nhầm lẫn.
A3.2. Các môi trường tổng quát cho nấm
Thạch nước cất (WA)
WA (2%) gồm 20g agar trong 1 L nước và được dùng làm giá thể cho bào tử nảy mầm trước khi cấy đơn bào tử. Sợi nấm mọc thưa thớt trên môi trường này vì vậy rất thích hợp làm môi trường nền cho việc cấy đỉnh sinh trưởng của sợi nấm để nuôi cấy các tản nấm mới. Việc nấm mọc thưa trên WA cũng thuận lợi cho việc phân lập nấm từ các bộ phận của cây, nhất là rễ.
Để cấy đơn bào tử và cấy đỉnh sinh trưởng của sợi nấm, nên đổ môi trường ra đĩa khi còn khá nóng nhằm làm cho môi trường được giàn mỏng trong đĩa - việc này hạn chế sự phát triển của nấm và giúp cho việc cắt bào tử hoặc đỉnh sợi nấm được dễ hơn.
WA (0,05%), 0,5 g agar trong 1 L nước, dùng để chuẩn bị chuỗi pha loãng đất. Một lượng nhỏ agar làm chậm dần quá trình lắng của các phần tử nấm. Agar được hòa tan trong nước trước khi được chia sang các chai McCartney. Nắp chai được nới lỏng trong khi khử trùng và đóng chặt sau khi hoàn tất khử trùng.
Thạch lá cẩm chướng (CLA) hoặc thạch với các giá thể thực vật tự nhiên khác
CLA là môi trường giá thể tự nhiên (Fisher et al. 1982) được chuẩn bị bằng cách để các miếng lá cẩm chướng tiệt trùng (khoảng 1 mẩu cho mỗi 2 mL thạch) trong một đĩa Petri và sau đó đổ WA 2% đã tiệt trùng vào.
Các miếng lá cẩm chướng được chuẩn bị từ lá tươi không có dư lượng thuốc trừ nấm hoặc thuốc trừ sâu. Ngay sau khi thu thập, lá được cắt thành những mẩu dài 5-8 mm và sấy khô trong tủ sấy có thông gió ở khoảng 70°C trong 3-4 giờ cho đến khi lá giòn. Có thể làm khô trong lò vi sóng. Những miếng lá khô được gói trong giấy nhôm hoặc hộp nhựa polycarbonate và khử trùng bằng phóng xạ gamma (25 kilograys). Các miếng lá đã được khử trùng có thể dự trữ ở 2-5°C tới 12 tháng trước khi dùng.
Nhiều loài nấm sinh bào tử trên môi trường CLA trong vòng 6 đến 10 ngày. Trên môi trường này, hình thái bào tử vô tính đồng nhất hơn so với khi dùng môi trường nhiều hydrat cacbon như PDA. Bào tử lớn của Fusarium tạo thành từng khối trên các mẩu lá. Nên sử dụng bào tử lớn hình thành trong các khối bào tử này cho việc giám định, vì chúng có hình dạng và chiều dài ổn định hơn so với bào tử lớn hình thành đơn độc từ cành bào tử phân sinh trên sợi nấm trong môi trường thạch. Bào tử nhỏ thường hình thành chủ yếu trên sợi nấm mọc trên mặt thạch, cách xa các mẩu lá. Cách thức hình thành các bào tử nhỏ, sự hiện diện các chuỗi bào tử nhỏ, và bào tử hậu có thể được xác định bằng cách kiểm tra trực tiếp trên kính hiển vi khi đĩa CLA nhỏ (đường kính 5 cm) được dùng cho việc giám định các mẫu nấm Fusarium. CLA cũng thích hợp cho việc sản sinh số lượng lớn bào tử cho các thí nghiệm.
 Nhiều bộ phận khác nhau của cây như các mẩu thân lúa xanh và quả đậu có thể thay thế cho lá cẩm chướng. Nếu cần thì khử trùng những mẩu cây này bằng nồi hấp. Bạn nên làm thí nghiệm để tìm ra loại vật liệu nào thích hợp nhất cho phòng thí nghiệm của bạn.
Nhiều bộ phận khác nhau của cây như các mẩu thân lúa xanh và quả đậu có thể thay thế cho lá cẩm chướng. Nếu cần thì khử trùng những mẩu cây này bằng nồi hấp. Bạn nên làm thí nghiệm để tìm ra loại vật liệu nào thích hợp nhất cho phòng thí nghiệm của bạn.
Thạch đường khoai tây (PDA)
PDA là môi trường nhiều hyđrat cacbon có chứa 20 g dextrose, 20 g agar và nước luộc 250 g khoai tây trắng, trong 1 lít nước. Khoai tây không gọt vỏ nhưng rửa sạch và cắt viên trước khi nấu cho vừa mềm. Khoai tây luộc chín được lọc qua vải thưa sao cho có một chút bã khoai tây trong nước luộc.
Bào tử vô tính hình thành trên PDA thường có hình dạng và kích thước không ổn định, và vì vậy ít được sử dụng trong việc giám định. Tuy nhiên, hình thái tản nấm, sự hình thành sắc tố và mức độ phát triển của nhiều loài nấm trên PDA khá ổn định, miễn là môi trường được chuẩn bị cẩn thận và mẫu vi sinh vật được nuôi cấy từ nguồn chuẩn và nuôi trong những điều kiện chuẩn. Đặc điểm của các tản được sử dụng như một đặc điểm phân loại thứ cấp. Mặc dù môi trường PDA được dùng để phân lập một số loài nấm bệnh, nhưng có nhiều loại nấm hoại sinh và vi khuẩn cũng phát triển nhanh trên PDA và có thể ức chế sự phát triển của tác nhân gây bệnh. Không nên dùng môi trường PDA cho việc phân lập, đặc biệt không dùng PDA để phân lập nguồn bệnh từ rễ.
Nên dùng PDA một phần tư độ mạnh cho các mục đích phân lập, có bổ sung kháng sinh khi phân lập từ mô thân hoặc lá.
Spezieller Nährstoffarmer Agar (SNA)
SNA là môi trường thạch nghèo dinh dưỡng, có thể dùng trong việc giám định và bảo quản các nguồn nấm Fusarium và Cylindrocarpon (Nirenberg 1976). Ngoài việc giúp hạn chế sự thoái hóa của mẫu nấm, môi trường này thúc đẩy sự hình thành bào tử nhỏ đồng đều. SNA được chuẩn bị bằng cách hấp khử trùng, trong 1L nước cất:
|
Agar |
20 g |
|
KH2PO4 |
1 g |
|
KNO3 |
1 g |
|
MgSO4.7H2O |
0.5 g |
|
KCl |
0.5 g |
|
Glucose |
0.2 g |
|
Sucrose |
0.2 g |
Đặt 2 mẩu giấy lọc đã khử trùng (1 cm vuông) lên trên mặt thạch sau khi đông, giúp thúc đẩy việc hình thành bào tử.
Vì SNA trong suốt, nên có thể dễ dàng quan sát mẫu nuôi cấy trực tiếp dưới kính hiển vi hoặc có thể đặt một mẫu nhỏ môi trường có chứa nấm vào trên lam kính, nhỏ một giọt nước, đậy lamen lại và quan sát dưới kính hiển vi. Môi trường SNA lỏng (không có agar) được dùng để nuôi cấy sinh khối sợi nấm cho việc tách DNA.
Thạch cà rốt khoai tây (PCA)
|
Cà rốt nghiền nhừ |
20 g |
|
Khoai tây nghiền nhừ |
20 g (khoai tây gọt vỏ) |
|
Agar |
20 g |
Gọt vỏ và cắt khoai tây, cà rốt thành những mẩu nhỏ. Bỏ vào trong một cốc đong có khoảng 200 mL nước cất và đun sôi nhỏ lửa trong 30 phút. Sau đó nghiền hai thứ qua một rây mịn hoặc xay nhuyễn. Thêm agar và nước cất cho đủ 1L. Lắc đều rồi hấp. Khi đổ môi trường nên lắc thường xuyên để cho cà rốt/khoai tây được trộn đều trong môi trường.
Cà rốt nhuyễn có nhiều sterol, cần thiết cho việc hình thành thể cái ở các loài nấm trứng. PCA là một môi trường quan trọng kích thích việc hình thành thể cái ở Pythium và Phytophthora.
A3.3. Môi trường chọn lọc nấm
Môi trường chọn lọc Phytophthora (PSM)
Công thức này có cả penicillin và ban đầu đã được TS. Nguyễn Vĩnh Trường gợi ý các tác giả dùng ở Việt Nam.
|
Agar |
8 g |
|
Cà rốt nghiền nhuyễn |
20 mL (công thức bên dưới) |
|
Khoai tây nghiền nhuyễn |
80 mL (công thức bên dưới) |
Đổ đầy thành 1 L bằng nước cất, hấp và khi nguội xuống 55°C, thêm:
|
Hymexazol |
3.7 mL dung dịch trong nước: |
|
Pimaricin |
400 µL |
|
Penicillin |
200 mg |
Bọc các đĩa môi trường bằng giấy nylon và cất trong tủ lạnh tránh tiếp xúc với ánh sáng. Loại bỏ môi trường sau một tháng. Đối với môi trường chọn lọc cho cả Phytophthora và Pythium, không sử dụng Hymexazol.
Cà rốt nghiền nhuyễn
Rửa, cắt viên 400 g cà rốt và hấp 10 phút trong 400 mL nước cất. Nghiền nhuyễn rồi thêm 500 mL nước. Có thể chia ra trong hộp nhựa và để ngăn đá đến khi cần dùng.
Khoai tây nghiền nhuyễn
Cắt viên 200 g khoai tây và đun trong 500 mL nước máy cho đến khi mềm. Nghiền nhuyễn và thêm nước cho đủ 800 mL. Cất giữ như trên.
Dung dịch mẹ Hymexazol
Cho 0,3 g hymexazol nguyên chất vào 20 mL nước tiệt trùng.
Pimaricin
Pimaricin có thể được trực tiếp thêm vào agar lỏng. Lắc đều trước khi dùng. Gói bằng giấy nhôm và dự trữ trong tủ lạnh.
Peptone PCNB Agar (PPA / môi trường Nash-Snyder)
PPA gồm có môi trường nền cộng thêm chất kháng sinh và thuốc trừ nấm, có thể dùng để phân lập chọn lọc các loài Fusarium từ đất pha loãng (Nash và Snyder 1962) hoặc từ các bộ phận cây. Môi trường này có khả năng ức chế hầu hết vi khuẩn và các loài nấm khác nhưng cho phép Fusarium mọc chậm, tạo thành các tản nấm nhỏ đường kính 5-10 mm sau 5-7 ngày.
Môi trường nền trong 1 L nước:
|
Agar |
20 g |
|
Peptone |
15 g |
|
KH2PO4 |
1 g |
|
MgSO4.7H20 |
0,5 g |
|
Terrachlor® |
1 g (chứa PCNB 75% w/w) |
Hấp môi trường nền và để nguội xuống 55oC trước khi thêm vào 10 mL nước vô trùng chứa:
Các đĩa môi trường đã chuẩn bị cần được 'để khô' trong chỗ tối và mát trước khi dùng sao cho phần nước trong dung dịch đất được thấm nhanh. Hầu hết các loài Fusarium không hình thành các tản nấm đặc trưng trên PPA; việc hình thành bào tử kém và hình thái bào tử vô tính không bình thường. Các tản nấm phải được cấy truyền và làm thuần cho việc giám định. Không nên duy trì mẫu Fusarium trên PPA bởi vì sự chuyển hóa của peptone dẫn đến việc tích tụ chất ammoniac độc.
PDA một phần tư độ mạnh có bổ sung kháng sinh.
Môi trường này được thiết kế chủ yếu là để phân lập các loài Fusarium từ mô cây, như thân cây bị nhiễm nấm F. oxysporum gây héo. Môi trường này cũng có thể được dùng cho một loạt các tác nhân khác, nhưng nên thử trước khi dùng cho một thí nghiệm quan trọng. PDA là một môi trường hữu dụng trong việc nghiên cứu chẩn đoán.
Không dùng môi trường này để phân lập Fusarium hoặc các loài nấm khác từ đất. 
Trong 1 L nước, trộn:
|
Chất chiết từ khoai tây |
Nước lọc từ 62,5 g khoai tây nấu |
|
Agar |
20 g |
|
Dextrose |
5 g |
|
PCNB (Terrachlor®) |
0.,1 g |
Hấp môi trường nền và để nguội xuống 55°C trước khi thêm, trong 10 mL nước sạch:
|
Streptomycin sulfate |
0,16 g |
|
Neomycin sulfate |
0,06 g |
Dichloran chloramphenicol peptone agar (DCPA)
DCPA được dùng cho việc phân lập chọn lọc các loài Fusarium và dematiaceous hyphomycetes từ hạt ngũ cốc (Andrews và Pitt 1986). Môi trường nền, trong 1 L nước cất, chứa:
|
Agar |
20 g |
|
Peptone |
15 g |
|
K2HPO4 |
1 g |
|
MgSO4.7H2O |
0,5 g |
|
Chloramphenicol |
0,2 g (chất kháng sinh phổ rộng - có thể hấp) |
Sau khi hấp, thêm, trong 10 mL ethanol:
|
Dichloran |
0,002 g |
Không nên dùng DCPA làm môi trường duy trì nấm bởi vì sự chuyển hóa của peptone dẫn đến việc tích tụ amoniac tới mức độ độc. Dichloran ngăn cản sự phát triển của nấm mucoraceous, và việc thiếu nguồn hyđrat cacbon trong môi trường cản trở sự phát triển của Aspergillus và Penicillium.
Môi trường lá lúa (hoặc lá cỏ) cho Pythium
Môi trường này hữu ích cho việc kích thích và quan sát sự hình thành bọc bào tử và thể cái ở nhiều loài Pythium. Bọc bào tử và thể cái hình thành từ sợi nấm mọc trên mặt nước gần các miếng lá. Môi trường này có thể được chuẩn bị bằng cách thả nổi các miếng lá lúa hay cỏ đã tiệt trùng trong đĩa Petri có nước:
1. Cắt lá lúa thành những mẩu dài 3cm.
2. Hấp và đặt 4-5 mẩu trong đĩa Petri lớn chứa 15 mL nước đã khử trùng.
3. Cấy một mẩu thạch chứa nguồn nấm vào môi trường.
Nấm sẽ phát triển trên các miếng lá, và sợi nấm sẽ mọc trên mặt nước. Để cố định nấm cho việc quan sát bằng kính hiển vi:
1. Đặt một miếng lamen dưới mặt nước.
2. Cẩn thận tách một chút sợi nấm và kéo lên trên lamen.
3. Lấy lamen ra khỏi môi trường, lật sấp, và đặt lên trên một lam kính có nhỏ sẵn một giọt nước.
A3.4. Môi trường dùng cho vi khuẩn
Môi trường King's B (KBM)
|
Agar |
15 g |
|
Proteose peptone số 3 |
20 g |
|
Glycerol, C.P. |
10 mL |
|
K2HPO4 |
1,5 g |
|
MgSO4 |
1,5 g |
|
Nước cất |
1L |
Trộn chung tất cả các thành phần ngoại trừ MgSO4. Chỉnh độ pH tới 7,2± 0,2. Từ từ thêm MgSO4 và lắc đều. Hấp và đổ vào đĩa Petri 90 mm.
Sucrose peptone agar (SPA)
|
Đường Sucrose |
20 g |
|
Peptone |
5 g |
|
K2HPO4 |
0,5 g |
|
MgSO4.7H2O |
0,25 g |
|
Agar |
20 g |
|
Nước cất |
1 L |
Trộn chung tất cả các thành phần. Chỉnh độ pH tới 7,2± 0,2. Hấp và đổ vào đĩa Petri 90 mm.
Môi trường Tetrazolium
Môi trường này (Kelman 1954) có thể được dùng để phân biệt giữa các tản nấm của loài Ralstonia solanacearum đột biến và nguyên chủng. Dạng đột biến thường hình thành các khuẩn lạc đỏ đậm, tròn với viền hẹp màu hơi xanh. Khuẩn lạc loại nguyên chủng có hình tròn khác thường, màu trắng, trông như dạng lỏng với trung tâm màu hồng.
|
Peptone |
10 g |
|
Casein hydrolysate |
1 g |
|
Glucose |
5 g |
|
Agar |
17 g |
|
Triphenyl tetrazolium chloride |
0,05 g |
|
Nước cất |
1 L |
Trộn chung tất cả các thành phần. Hấp và đổ vào đĩa Petri 90 mm.
A3.5. Khử trùng
Khử trùng là quá trình tiêu diệt tất cả các vi sinh vật trong môi trường nuôi cấy hoặc trên bề mặt dụng cụ thủy tinh dùng trong các công việc cần vô trùng, như các đĩa Petri thủy tinh.
Khử trùng bằng nhiệt
Nhiệt độ và thời gian cần thiết để tiêu diệt vi sinh vật tỷ lệ nghịch với nhau. Bảng A3.2 cho thấy thời gian tối thiểu cần cho khử trùng hiệu quả ở các mức nhiệt độ cho cả hai loại nóng ẩm và nóng khô:
Bảng A3.2. Thời gian cần cho việc khử trùng nóng ẩm và nóng khô ở các mức nhiệt độ khác nhau
|
Nhiệt độ |
Nóng ẩm |
Nóng khô |
|
100 °C |
20 giờ |
|
|
110 °C |
2,5 giờ |
|
|
121 °C |
15 phút |
8,0 giờ |
|
130 °C |
2,5 phút |
|
|
140 °C |
2,5 giờ |
Những thời gian này không bảo đảm tiệt trùng hoàn toàn. Đó là những mức thời gian được tính toán dựa trên kinh nghiệm và mức độ lẫn tạp bình thường của các vi sinh vật chịu nhiệt.
Loài, chủng và khả năng hình thành bào tử của vi sinh vật ảnh hưởng rất lớn đến tính mẫn cảm của vi sinh vật đối với nhiệt. Trong điều kiện khử trùng bằng nồi hấp, các dạng sinh trưởng sinh dưỡng của hầu hết các loại vi khuẩn, nấm men, nấm và hầu hết các virút gây bệnh động vật bị tiêu diệt trong khoảng nhiệt độ từ 50oC đến 60oC trong 10 phút. Tuy nhiên các bào tử vi khuẩn cần 15 phút ở nhiệt độ từ 100°C đến 121°C. Trong điều kiện nóng khô các bào tử vi khuẩn cần 1 giờ ở 160°C.
Tính chất của vật liệu trong đó vi sinh vật được khử trùng bằng nhiệt cũng là một yếu tố quan trọng. Hàm lượng các chất hữu cơ cao thường có khuynh hướng bảo vệ bào tử và các vi sinh vật sinh dưỡng chống lại tác động của nhiệt độ. Chất đạm, gelatin, đường, tinh bột, axít nuclêic, mỡ và dầu đều tác động cách này. Tác động của mỡ và dầu mạnh nhất trong điều kiện nóng ẩm bởi vì các chất này ngăn không cho hơi ẩm tiếp xúc với vi trùng. Độ pH cũng rất quan trọng. Sự chịu nhiệt của bào tử vi khuẩn cao nhất ở pH trung tính và giảm khi tăng độ axít hoặc độ kiềm.
Khử trùng nóng khô
Điều kiện nóng khô tiêu diệt vi trùng bằng quá trình oxi hóa. Quá trình nhiệt khô là phương pháp tốt nhất để khử trùng đồ thủy tinh khô như ống nghiệm, đĩa Petri thủy tinh, bình tam giác, pipet, tất cả các ống tiêm thủy tinh và dụng cụ như kẹp, dao mổ và kéo.
 Đồ thủy tinh cần được gói lại sao cho hơi nóng đi vào được mọi chỗ cần sấy. Quá trình này được hỗ trợ bằng hệ thống quạt trong tủ sấy. Thời gian cần cho khử trùng là 160°C trong 1 giờ. Tuy nhiên hầu hết các tủ sấy, nhất là khi để nhiều, cần 2 đến 3 giờ mới đạt nhiệt độ. Như vậy 4 giờ ở 160°C là tối thiểu cho một lô dụng cụ lớn. Bốn tiếng đồng hồ ở 170°C là ranh giới an toàn.
Đồ thủy tinh cần được gói lại sao cho hơi nóng đi vào được mọi chỗ cần sấy. Quá trình này được hỗ trợ bằng hệ thống quạt trong tủ sấy. Thời gian cần cho khử trùng là 160°C trong 1 giờ. Tuy nhiên hầu hết các tủ sấy, nhất là khi để nhiều, cần 2 đến 3 giờ mới đạt nhiệt độ. Như vậy 4 giờ ở 160°C là tối thiểu cho một lô dụng cụ lớn. Bốn tiếng đồng hồ ở 170°C là ranh giới an toàn.
 Không được mở tủ sấy trong thời gian sấy bởi vì mở cửa trong vài giây có thể khiến nhiệt độ giảm tới 70°C, mà phải cần cả giờ sau đó để tủ sấy trở lại nhiệt độ mong muốn. Việc này sẽ làm cho lô dụng cụ đó không được khử trùng.
Không được mở tủ sấy trong thời gian sấy bởi vì mở cửa trong vài giây có thể khiến nhiệt độ giảm tới 70°C, mà phải cần cả giờ sau đó để tủ sấy trở lại nhiệt độ mong muốn. Việc này sẽ làm cho lô dụng cụ đó không được khử trùng.
Khử trùng nóng ẩm
Nóng ẩm tiêu diệt vi sinh vật, có thể qua việc làm đông và làm biến tính enzym và protêin cấu trúc của chúng, một quá trình cần có nước. Vì vậy tất cả các môi trường nuôi cấy được khử trùng nóng ẩm bằng cách dùng nồi hấp.
|
Nếu dùng nồi áp suất hoặc nồi hấp không tự động, để hơi nước xì ra ở van thoát hơi khoảng 2-3 phút trước khi đóng van hoặc vặn nắp. Phải dùng rổ thay vì hộp và không được hấp pipet trong hộp đựng bởi vì các túi không khí bên trong khiến việc khử trùng mất hiệu lực. Nhiệt độ chứ KHÔNG PHẢI áp suất là tiêu chí thực sự quyết định sự thành công của quá trình khử trùng. Nồi hấp phải được chỉnh sao cho áp suất không giảm quá nhanh bởi vì sẽ dẫn đến hiện tượng môi trường sôi tràn và làm ướt nắp đậy. Môi trường cần để yên trong nồi khoảng 5 phút sau khi nồi trở lại áp suất không khí, bởi vì đôi khi các dung dịch còn ở trong tình trạng quá nóng và có thể bắn môi trường hoặc agar đang sôi lên người, gây ra bỏng. Nếu để trong nồi hấp quá lâu, sẽ mất bớt thể tích do chân không tích tụ trong nồi hấp. |
Không nên hấp những bình chứa môi trường lớn nhỏ khác nhau cùng một mẻ bởi vì các lượng lớn cần nhiều thời gian hơn để đạt được nhiệt độ cần thiết, như vậy sẽ làm cho các lượng nhỏ nhận quá nhiều nhiệt. Bảng A3.3 đưa ra chỉ dẫn về thời gian cần thêm để đạt nhiệt độ mong muốn:
Bảng A3.3. Thời gian khuyến cáo để khử trùng các lượng dung dịch khác nhau
|
Thể tích dung dịch |
Thời gian thêm (phút) |
Tổng cộng thời gian ở 121°C |
|
chai 100 mL |
10 |
25 |
|
chai 250 mL |
12 |
27 |
|
chai 500 mL |
18 |
33 |
|
chai 1000 mL |
22 |
37 |
|
chai 2000 mL |
27 |
42 |
Khử trùng dụng cụ
Kẹp, que cấy và các dụng cụ khác phải được khử trùng trước khi tiếp xúc với mẫu cấy nhằm tránh lẫn tạp. Que cấy được khử trùng tốt nhất bằng cách hơ cho nóng đỏ trên ngọn lửa.
 Phải để que cho nguội xuống nhiệt độ phòng trước khi dùng. Que cấy nóng là nguyên nhân phổ biến làm cho việc cấy truyền, cấy đỉnh sợi nấm và cấy đơn bào tử bị thất bại.
Phải để que cho nguội xuống nhiệt độ phòng trước khi dùng. Que cấy nóng là nguyên nhân phổ biến làm cho việc cấy truyền, cấy đỉnh sợi nấm và cấy đơn bào tử bị thất bại.
Kẹp và dao được khử trùng bằng cách nhúng vào cồn. Trước khi dùng, đốt sạch cồn bằng cách hơ qua ngọn lửa để cồn bốc cháy. Đừng giữ dụng cụ trên ngọn lửa vì sẽ làm cho dụng cụ quá nóng. Cẩn thận không đặt các dụng cụ nóng hoặc hơ lửa dung cụ trong hoặc gần cồn vì có thể gây hỏa hoạn.
Khử trùng bề mặt nơi làm việc
Khay, bàn và các bề mặt khác có thể được khử trùng với dung dịch khử trùng. Cồn là dung dịch thường được dùng nhất. Cồn pha nước là chất khử trùng tốt nhất, thích hợp nhất là cồn 70%. Cồn mêthyl cũng có thể sử dụng để khử trùng.
A3.6. Bảo quản mẫu cấy
Bảo quản mẫu vi sinh vật sống
Mẫu vi sinh vật sống được lưu giữ dùng làm mẫu tham khảo, hoặc để sau này dùng trong quá trình lây bệnh nhân tạo hoặc các thí nghiệm khác. Các mẫu vi sinh vật lưu trữ trong bộ sưu tập mẫu vi sinh vật quốc gia là một phần các vật liệu tham khảo nhằm hỗ trợ cơ sở dữ liệu quốc gia về tác nhân gây bệnh cây.
Bảo quản trong nước cất—Pythium và Phytophthora
Đây là một phương pháp đơn giản và ít tốn kém đặc biệt thích hợp cho Pythium và Phytophthora. Nên sử dụng tủ cấy vô trùng để thực hiện quy trình giữ mẫu này. Cắt các mẩu thạch vuông 1 cm từ viền của một tản nấm mọc mạnh và còn mới. Đặt những miếng thạch có chứa nấm này vào trong một lọ McCartney có chứa nước vô trùng và vặn chặt nắp. Lọ bảo quản được để nơi mát. Không bảo quản trong tủ lạnh bởi vì một số loài bị chết ở nhiệt độ thấp. Các mẫu có thể được cất giữ từ 6 tháng đến 2 năm, tùy theo loài. Các mẫu được hồi phục bằng cách lấy một miếng thạch từ lọ và cấy lên môi trường mới sao cho mặt có nấm tiếp xúc với bề mặt môi trường. Cần đảm bảo là nước và các miếng thạch không bị tạp vi khuẩn— sự có mặt của vi khuẩn sẽ làm cho nấm chết nhanh chóng.
Bảo quản hạch nấm
Hạch nấm có thể được lưu giữ trong thời gian dài ở điều kiện khô mát trong một lọ thủy tinh nhỏ có nắp vặn. Đây là kỹ thuật thích hợp để lưu giữ các loài như Sclerotium rolfsii, Sclerotinia sclerotiorum, Rhizoctonia spp. (các loài tạo hạch nấm).
Tại các vùng nhiệt đới thì tốt nhất nên lưu giữ hạch nấm trên giấy thấm tiệt trùng đặt bên trên silica gel màu xanh trong lọ McCartney (hoặc lọ có nắp vặn tương tự) để đảm bảo ẩm độ thấp trong quá trình bảo quản.
Bảo quản các mẩu thân hoặc lá bị bệnh.
Các mẫu vi sinh vật được nuôi cấy trên WA tiệt trùng có chứa các mẩu mô cây hoặc hạt tiệt trùng. Các mẩu mô thực vật có chứa vi sinh vật được làm khô rồi cất giữ trong các ống thủy tinh nhỏ. Một cách khác, các mẫu này có thể được bảo quản trong lọ kín trên giấy thấm vô trùng đặt bên trên lớp silica gel màu xanh để đảm bảo điều kiện bảo quản luôn khô.
Để có thông tin sâu rộng hơn về việc bảo quản các mẫu vi sinh vật, tham khảo Shivas and Beasley (2005), Quản lý mẫu bệnh thực vật.
Làm đông khô
Làm đông khô là phương pháp chọn lựa cho quá trình bảo quản lâu dài nhiều loại nấm và thường được dùng ở hầu hết các nơi quan trọng lưu giữ mẫu vi sinh vật. Điều trở ngại chính là cần có các thiết bị chuyên môn tốn kém. Phương pháp này thích hợp nhất cho những loài nấm mọc và sinh bào tử tốt trên mô cây tiệt trùng như các mẩu thân lúa xanh hoặc mẩu lá cẩm chướng. Cũng có nhiều loài nấm không thể bảo quản bằng phương pháp đông khô, như nấm trứng, gỉ sắt và sương mai.
Các mẫu nuôi cấy được làm đông khô bằng cách làm khô các miếng lá hoặc thân có chứa mẫu vi sinh vật trong các ống thuỷ tinh nhỏ trong điều kiện chân không cao (10-1 đến 10-2 Torr). Các ống thủy tinh được nút bằng một miếng bông gòn nhỏ và hấp trong một cốc đong đậy nắp sơ. Lấy năm mẩu lá hoặc thân từ mẫu nuôi cấy (sau hai tuần nuôi cấy từ đơn bào tử), và dùng dụng cụ vô trùng chuyển sang ống thủy tinh. Ống được đóng lại sau khi đã cho nhãn vào trong lọ, sau đó dùng đèn hàn hơ lửa và kéo dài ống ra thành hình dạng như đồng hồ cát. Ống được gắn vào máy đông khô và vận hành máy trong 12-24 giờ, rồi hàn kín dưới điều kiện chân không cao và bảo quản ở nhiệt độ thường hoặc ở 5°C. Nhiều loài Fusarium và các chi nấm khác đã được làm đông khô thành công với kỹ thuật này và được bảo quản trong nhiều năm.
Các mẫu vi sinh vật này có thể được hồi phục bằng cách cấy các mẩu lá hoặc thân đã làm đông khô lên một môi trường thích hợp. Ống thủy tinh chứa mẫu bảo quản phải được khử trùng bề mặt trước khi đập vỡ để lấy các mẩu lá.
Các phương pháp bảo quản mẫu vi sinh vật sống khác
Để bảo quản được lâu, các mẫu vi sinh vật cũng có thể được lưu giữ dưới dạng dung dịch bào tử trong glycerol ở -80°C. Nhiều loài cũng có thể được lưu giữ thành công trong nitơ lỏng. Tuy nhiên, những phương pháp này rất tốn kém.
Bảo quản mẫu nấm cho mục đích duy trì dữ liệu tiêu bản mẫu
Các mẫu gốc nuôi cấy trên môi trường PDA phải được nộp đến một trung tâm lưu giữ tiêu bản mẫu được thế giới công nhận khi việc mô tả chính thức một loài mới được công bố.
Các mẫu được nuôi cấy từ đơn bào tử nảy mầm và phát triển trong điều kiện nhiệt độ và ánh sáng bình thường từ 2 đến 3 tuần. Mẫu nuôi cấy sau đó được xử lý chết bằng cách để đĩa tiếp xúc với dung dịch formalin trong một hộp kín trong 3 ngày. Mẫu sau đó được bảo quản bằng cách dùng agar và glycerine. Ba gram agar hòa tan trong 147 mL nước, sau đó được chia thành những phần 6 mL bỏ trong ống nghiệm trước khi hấp. Lật ngược nắp đĩa mẫu nuôi cấy, cho 1,5-1,75 mL glycerine và 6 mL thạch nóng lên trên glycerine. Dùng dụng cụ vô trùng nhấc mẫu nuôi cấy từ đĩa Petri lên và đặt lên trên hỗn hợp ở nắp đĩa. Các mẫu nuôi cấy sau đó được để cho khô trong ngăn kéo 3-5 ngày, che bằng một mảnh giấy. Khi khô, mẫu dẻo như cao su và có thể lấy ra khỏi đĩa Petri để lưu trữ. Quy trình này đầu tiên được phát triển để bảo quản các loài Fusarium ở Trung tâm Nghiên cứu Fusarium, Đại học Bang Pennsylvania. Quy trình này cũng phù hợp với nhiều loại nấm.
Bảo quản nấm trong dầu khoáng
Nhiều mẫu nấm có thể được bảo quản trong dầu khoáng (paraffin) tới 4-5 năm ở 15-20°C. Các mẫu nên được nuôi cấy trên môi trường PDA có thêm 0,1% yeast extract (như Vegemite®). Dầu khoáng được chuẩn bị như sau:
1. Đổ 11 mL dầu paraffin vào chai McCartney 25 mL không có nắp cao su.
2. Đậy nắp lỏng và hấp khử trùng ở 121°C trong 20 phút.
3. Để cho hoàn toàn nguội trong nồi hấp.
4. Lấy nước khỏi dầu nếu có, bằng cách làm nóng trong tủ sấy ở 120°C trong 8 giờ và để nguội dần trong tủ sấy qua đêm xuống nhiệt độ thường. Loại bỏ bất cứ lọ nào có dầu vẩn đục hoặc thực hiện lại quá trình làm nóng trong tủ sấy.
Các mẫu nấm cần được nuôi cấy trên mặt nghiêng môi trường PDA có thêm yeast extract trong lọ McCartney 25mL (không có nắp cao su) cho đến khi nấm mọc bao phủ toàn bộ bề mặt môi trường. Để bảo quản mẫu nuôi cấy, dùng dụng cụ vô trùng thêm 11 mL dầu thô đã khử trùng vào từng mẫu trong trong tủ cấy vô trùng. Ghi nhãn cẩn thận với số mẫu và ngày cất giữ
Các mẫu vi sinh vật có thể được cấy lại như sau:
1. Dùng dụng cụ tiệt trùng lấy một miếng thạch nhỏ từ mẫu bảo quản. .
2. Thấm dầu với giấy lọc hoặc giấy thấm tiệt trùng.
3. Cấy mẩu thạch lên một môi trường thích hợp.
Ghi chú: Mỗi lần nên bảo quản ba mẫu từ mỗi nguồn nấm, và mẫu bảo quản trong dầu thô cần được thay thế sau 4-5 năm.
Các tác giả chân thành cảm ơn N.J. Cother và M.J. Priest qua những đóng góp về mặt kỹ thuật này của họ.
Tài liệu tham khảo
Andrews S. and Pitt J.I. 1986. Selective medium for isolation of Fusarium species and dematiaceous hyphomycetes from cereals. Applied Environmental Microbiology 51(6), 1235-1238.
Fisher N.L., Burgess L.W., Toussoun T.A. and Nelson P.E. 1982. Carnation leaves used as a substrate and for the preservation of cultures of Fusarium species. Phytopathology 72, 151-153.
Kelman A. 1954. The relationship of pathogenicity in Pseudomonas solanacearum to colony appearance on tetrazolium medium. Phytopathology 44, 693-694.
Nash S.M. and Snyder W.C. 1962. Quantitative estimations by plate counts of propagules of the bean root rot Fusarium in field soils. Phytopathology 52, 567-572.
Nirenberg H.I. 1976. Untersuchungen uber die morphologische und biologische differenzierung der Fusarium section liseola. Mitt Biol Bundesanst Land. Forstw Berlin-Dahlem.
Shivas R. and Beasley D. 2005. Management of plant pathogen collections. Australian Government Department of Agriculture, Fisheries and Forestry. At: <http://www.daff.gov.au/planthealth>.
Cuốn cẩm nang này được sắp xếp thành các phần sau:
- Phần 1: Phần giới thiệu
-
Phần 2: Tổng quát về sức khỏe thực vật và các yếu tố ảnh hưởng
-
Phần 3: Quy trình chẩn đoán tác nhân gây bệnh trong phòng thí nghiệm và ngoài đồng ruộng
-
Phần 4: Các triệu chứng bệnh cây
-
Phần 5: Quy trình và thiết bị làm việc trên đồng ruộng
-
Phần 6: Quy trình và thiết bị làm việc trong phòng thí nghiệm
-
Phần 7: Giới thiệu sơ lược về phân loại nấm
-
Phần 8: Các phương pháp lây bệnh nhân tạo
-
Phần 9: Quản lý bệnh hại tổng hợp
-
Phần 10: Các bệnh do nấm có nguồn gốc từ đất
-
Phần 11: Các bệnh thường gặp trên một số cây trồng có ý nghĩa kinh tế
-
Phần 12: Ảnh hưởng sức khỏe từ nấm gây bệnh
-
Phần 13: Thiết kế, xây dựng và vận hành các phòng thí nghiệm và nhà lưới dùng cho chẩn đoán
- Phần 14: Phụ lục về cách làm que cấy dẹp, sức khỏe an toàn trong công việc, cũng như các công thức nấu môi trường, các phương pháp khử trùng, và các phương pháp lưu giữ mẫu nấm.
-
Cẩm nang bệnh cây - P11: Các bệnh phổ biến trên một số cây trồng quan trọng
 Việc chẩn đoán chính xác tác nhân gây bệnh là vô cùng cần thiết trước khi đưa ra biện pháp quản lý bệnh hại tổng hợp. Chẳng hạn như thối rễ do nấm có thể do nhiều tác nhân...
Việc chẩn đoán chính xác tác nhân gây bệnh là vô cùng cần thiết trước khi đưa ra biện pháp quản lý bệnh hại tổng hợp. Chẳng hạn như thối rễ do nấm có thể do nhiều tác nhân... -
Cẩm nang bệnh cây - P12: Nấm, người và động vật: các vấn đề về sức khỏe
 Một số nấm gây bệnh trên người và các động vật khác - những bệnh này được gọi là các bệnh nấm. Chẳng hạn như Aspergilllus flavus có thể xâm nhiễm vào phổi người, gây ra...
Một số nấm gây bệnh trên người và các động vật khác - những bệnh này được gọi là các bệnh nấm. Chẳng hạn như Aspergilllus flavus có thể xâm nhiễm vào phổi người, gây ra... -
Cẩm nang bệnh cây - P13: Phòng thí nghiệm chẩn đoán và nhà lưới
 Thiết kế và bố trí và chuẩn bị thiết bị cho phòng thí nghệm chuẩn đoán bệnh cây, chuẩn bị và xây dựng nhà lưới cho việc nghiên cứu bệnh cây, Các pha dung dịch Hoagland's...
Thiết kế và bố trí và chuẩn bị thiết bị cho phòng thí nghệm chuẩn đoán bệnh cây, chuẩn bị và xây dựng nhà lưới cho việc nghiên cứu bệnh cây, Các pha dung dịch Hoagland's...
-
 Công dụng của giấm gỗ đối với cây trồng trong nông nghiệp
Công dụng của giấm gỗ đối với cây trồng trong nông nghiệp
-
 Vai trò cân bằng Auxin – GA – Cytokinin trong phân hóa mầm hoa thanh long
Vai trò cân bằng Auxin – GA – Cytokinin trong phân hóa mầm hoa thanh long
-
 Paclobutrazole là gì? Cơ chế, ứng dụng và lưu ý quan trọng trong sản xuất nông nghiệp
Paclobutrazole là gì? Cơ chế, ứng dụng và lưu ý quan trọng trong sản xuất nông nghiệp
-
 Phác đồ xử lý ra hoa vải U Hồng hiệu quả cao theo từng giai đoạn sinh lý
Phác đồ xử lý ra hoa vải U Hồng hiệu quả cao theo từng giai đoạn sinh lý
-
 Vì sao cây trồng sinh trưởng kém dù chăm sóc đầy đủ?
Vì sao cây trồng sinh trưởng kém dù chăm sóc đầy đủ?
-
 Khi nào nên bón vôi cho đất và những lưu ý quan trọng
Khi nào nên bón vôi cho đất và những lưu ý quan trọng
 Danh mục cây trồng
Danh mục cây trồng Côn trùng hại cây trồng
Côn trùng hại cây trồng Bệnh hại cây trồng
Bệnh hại cây trồng Dinh dưỡng cây trồng
Dinh dưỡng cây trồng Bài chuyên mục
Bài chuyên mục Liên hệ
Liên hệ


 Cây mai chiếu thủy
Cây mai chiếu thủy
 Cây đào
Cây đào
 Cây hoa hồng
Cây hoa hồng
 Cây nhãn
Cây nhãn
 COMBO COMBI 05: Biến vàng thành xanh
COMBO COMBI 05: Biến vàng thành xanh
 COMBO T-ROOT kích rễ toàn diện - phục hồi cây yếu, thúc rễ cực mạnh
COMBO T-ROOT kích rễ toàn diện - phục hồi cây yếu, thúc rễ cực mạnh
 Sử dụng kết hợp đạm Ure và Atonik đậm đặc - 'Công thức vàng' trong sử dụng phân bón
Sử dụng kết hợp đạm Ure và Atonik đậm đặc - 'Công thức vàng' trong sử dụng phân bón
 Những tác dụng và tính năng nổi bật khi sử dụng Cytokinin DA6 trên cây trồng
Những tác dụng và tính năng nổi bật khi sử dụng Cytokinin DA6 trên cây trồng
 Làm cách nào để ngăn chặn lộc, đọt non trên cây trồng?
Làm cách nào để ngăn chặn lộc, đọt non trên cây trồng?
 Hướng dẫn kích thích hoa ly nở và kìm hãm hoa cúc nở vào đúng dịp Tết
Hướng dẫn kích thích hoa ly nở và kìm hãm hoa cúc nở vào đúng dịp Tết
 Làm cách nào để cây hoa cúc phát triển nhanh và nở hoa đúng thời điểm?
Làm cách nào để cây hoa cúc phát triển nhanh và nở hoa đúng thời điểm?
 Cơ chế hút nước và dinh dưỡng của cây trồng
Cơ chế hút nước và dinh dưỡng của cây trồng
 Đất là gì? khái niệm về đất, bản chất và thành phần của đất
Đất là gì? khái niệm về đất, bản chất và thành phần của đất
 Quá trình hấp thụ và vận chuyển khoáng trong cây trồng
Quá trình hấp thụ và vận chuyển khoáng trong cây trồng
 Đất mặn và ảnh hưởng của đất mặn đến sự phát triển của cây trồng
Đất mặn và ảnh hưởng của đất mặn đến sự phát triển của cây trồng

 Trang chủ
Trang chủ
 Cây trồng phong thủy
Cây trồng phong thủy
 Cây CN dài ngày
Cây CN dài ngày
 Cây CN ngắn ngày
Cây CN ngắn ngày
 Cây lương thực
Cây lương thực
 Cây rau màu
Cây rau màu
 Cây ăn quả (trái)
Cây ăn quả (trái)
 Cây cảnh, hoa cảnh
Cây cảnh, hoa cảnh
 Cây thuốc (dược liệu)
Cây thuốc (dược liệu)
 Cây lâm nghiệp
Cây lâm nghiệp
 Cẩm nang phân bón
Cẩm nang phân bón
 Trồng trọt, chăm sóc
Trồng trọt, chăm sóc
 Khoa học nông nghiệp
Khoa học nông nghiệp
 Sức khỏe và làm đẹp
Sức khỏe và làm đẹp

